Ядра атомов: в самом сердце материи
Экология потребления. Наука и техника: Ядро атома получается крохотным, его радиус в 10 000–100 000 раз меньше всего атома. Отметим, что протоны и нейтроны вместе часто называют «нуклонами», а Z+N часто называют A – общее количество нуклонов в ядре. Также Z, «атомное число» – количество электронов в атоме.
Ядро атома получается крохотным, его радиус в 10 000–100 000 раз меньше всего атома. Каждое ядро содержит определённое количество протонов (обозначим его Z) и определённое количество нейтронов (обозначим его N), скреплённых вместе в виде шарика, по размеру не сильно превышающего сумму их размеров. Отметим, что протоны и нейтроны вместе часто называют «нуклонами», а Z+N часто называют A – общее количество нуклонов в ядре. Также Z, «атомное число» – количество электронов в атоме.
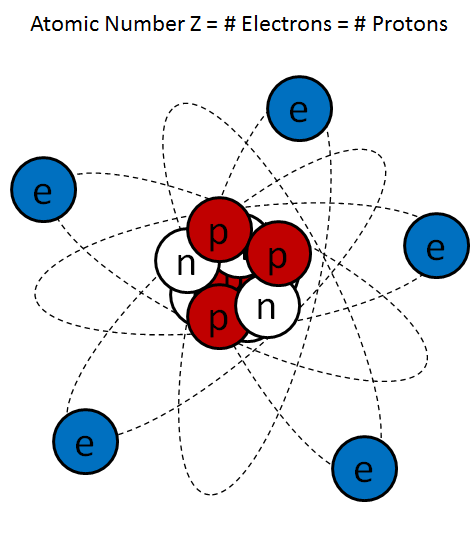
Рис. 1
Типичное мультяшное изображение атома (рис. 1) чрезвычайно преувеличивает размер ядра, но более-менее правильно представляет ядро как небрежно соединённое скопление протонов и нейтронов.
Содержимое ядра
Откуда нам известно, что находится в ядре? Эти крохотные объекты просто охарактеризовать (и это было просто исторически) благодаря трём фактам природы.
1. Протон и нейтрон отличаются по массе всего лишь на тысячную часть, так что если нам не нужна чрезвычайная точность, можно сказать, что у всех нуклонов масса одинакова, и назвать её массой нуклона, mнуклон:
mпротон ≈ mнейтрон ≈ mнуклон
(≈ означает «примерно равно»)
2. Количество энергии, необходимой для удержания вместе протонов и нейтронов в ядре, относительно мало – порядка тысячной доли части энергии массы (E = mc2) протонов и нейтронов, так что масса ядра почти равна сумме масс его нуклонов:
Mядро ≈ (Z+N) × mнуклон
3. Масса электрона равняется 1/1835 массы протона – так что почти вся масса атома содержится в его ядре:
Mатом ≈ Mядро
Тут подразумевается наличие четвёртого важного факта: все атомы определённого изотопа определённого элемента одинаковы, как и все их электроны, протоны и нейтроны.
Поскольку в самом распространённом изотопе водорода содержится один электрон и один протон:
Mводород ≈ mпротон ≈ mнуклон
масса атома Mатом определённого изотопа просто равна Z+N, помноженному на массу атома водорода
Mатом ≈ Mядро ≈ (Z+N) × mнуклон ≈ (Z+N) × Mводород
и погрешность этих уравнений примерно равна 0,1%.
Поскольку нейтроны электрически нейтральны, электрический заряд Qядро ядра просто равен количеству протонов, помноженному на электрический заряд протона («e»):
Qядро = Z × Qпротон = Z × e
В отличие от предыдущих уравнений, это уравнение выполняется точно.
Подытожим:
Z = Qядро / e
A = Z + N ≈ Mатом / Mводород
Эти уравнения проиллюстрированы на рис. 2
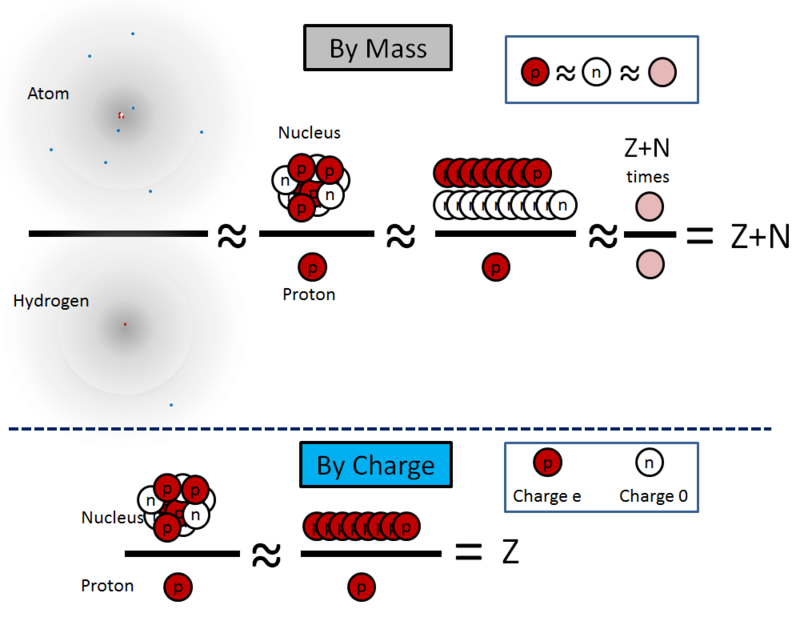
Рис. 2
Используя открытия последних десятилетий XIX века и первых десятилетий XX, физики знали, как измерить в эксперименте оба обозначенных красным значения: заряд ядра в e, и массу любого атома в атомах водорода. Так что эти значения были известны уже в 1910-х. Однако правильно интерпретировать их смогли только в 1932 году, когда Джеймс Чедвик определил, что нейтрон (идею которого предложил Эрнест Резерфорд в 1920-м) является отдельной частицей. Но как только стало понятно, что нейтроны существуют, и что их масса практически равна массе протона, сразу же стало ясно, как интерпретировать числа Z и N — количество протонов и нейтронов. А также сразу родилась новая загадка – почему у протонов и нейтронов почти одинаковая масса.
Честно говоря, физикам того времени с научной точки зрения страшно повезло, что всё это было так легко установить. Закономерности масс и зарядов настолько просты, что даже самые долгие загадки были раскрыты сразу после открытия нейтрона. Если бы хотя бы один из перечисленных мною фактов природы оказался неверным, тогда на то, чтобы понять, что происходит внутри атомов и их ядер, ушло бы гораздо больше времени.
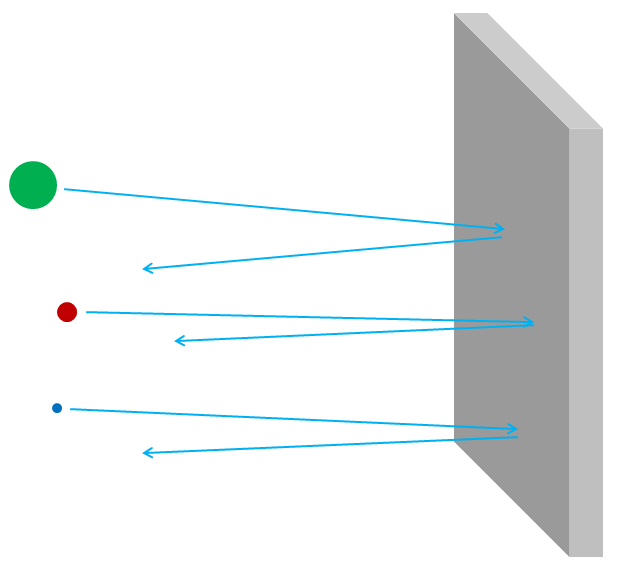
Рис. 3
К сожалению, с других точек зрения было бы гораздо лучше, если бы всё оказалось сложнее. Вряд ли можно было подобрать худший момент для этого научного прорыва. Открытие нейтрона и понимание структуры атома совпало с мировым экономическим кризисом, известным, как Великая Депрессия, и с появлением нескольких авторитарных и экспансионистских правительств в Европе и Азии. Быстро началась гонка ведущих научных держав в области понимания и получения энергии и оружия из ядра атома. Реакторы, выдающие ядерную энергию, были получены всего за десять лет, а за тринадцать – ядерное оружие. И сегодня нам приходится жить с последствиями этого.
Откуда нам известно, что ядро атома маленькое?
Одно дело – убедить себя, что определённое ядро определённого изотопа содержит Z протонов и N нейтронов; другое – убедить себя, что ядра атомов крохотные, и что протоны с нейтронами, будучи сжатыми вместе, не размазываются в кашу и не разбалтываются в месиво, а сохраняют свою структуру, как подсказывает нам мультяшное изображение. Как это можно подтвердить?
Я уже упоминал, что атомы практически пусты. Это легко проверить. Представьте себе алюминиевую фольгу; сквозь неё ничего не видно. Поскольку она непрозрачная, вы можете решить, что атомы алюминия:
1. Настолько крупные, что между ними нет просветов,
2. Настолько плотные и твёрдые, что свет сквозь них не проходит.
Насчёт первого пункта вы будете правы; в твёрдом веществе между двумя атомами почти нет свободного пространства. Это можно наблюдать на изображениях атомов, полученных при помощи особых микроскопов; атомы похожи на маленькие сферы (краями которых служат края электронных облаков), и они довольно плотно упакованы. Но со вторым пунктом вы ошибётесь.
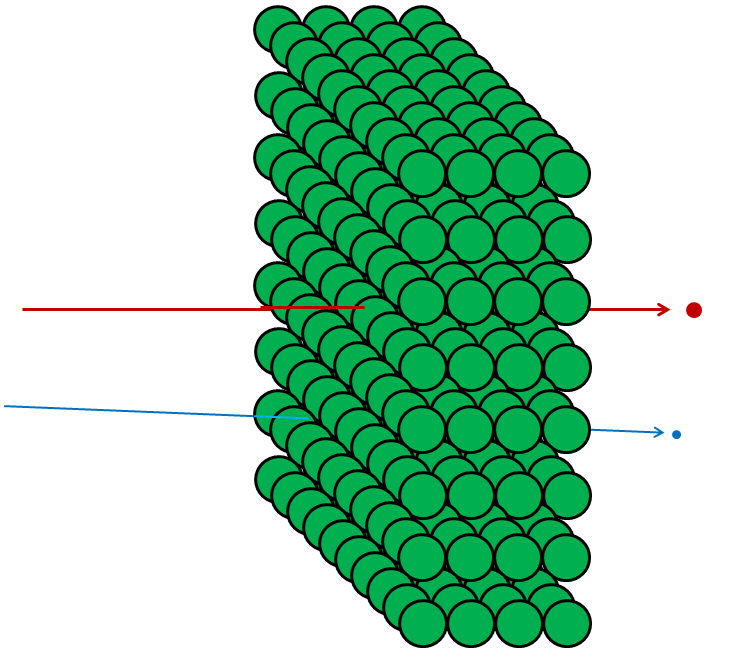
Рис. 4
Если бы атомы были непроницаемыми, тогда сквозь алюминиевую фольгу ничто не смогло бы пройти – ни фотоны видимого света, ни рентгеновские фотоны, ни электроны, ни протоны, ни атомные ядра. Всё, что вы направили бы в сторону фольги, либо застревало бы в ней, либо отскакивало бы – точно так же, как любой кинутый объект должен отскочить или застрять в гипсокартонной стенке (рис. 3). Но на самом деле электроны высокой энергии легко могут пройти через кусочек алюминиевой фольги, как и рентгеновские фотоны, высокоэнергетические протоны, высокоэнергетические нейтроны, высокоэнергетические ядра, и так далее. Электроны и другие частицы – почти все, если точнее – могут пройти через материал, не потеряв ни энергии, ни импульса в столкновениях с чем-либо, содержащимся внутри атомов. Лишь малая часть их ударится об атомное ядро или электрон, и в этом случае они могут потерять большую часть своей начальной энергии движения. Но большая часть электронов, протонов, нейтронов, рентгеновских лучей и всякого такого просто спокойно пройдут насквозь (рис. 4). Это не похоже на швыряние гальки в стену; это похоже на швыряние гальки в сетчатый забор (рис. 5).
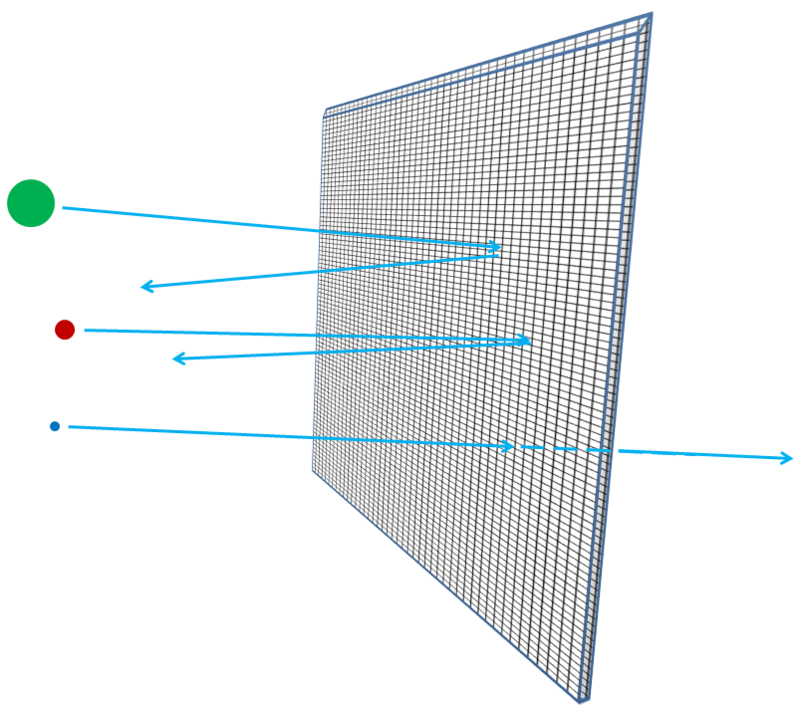
Рис. 5
Чем толще фольга – к примеру, если складывать всё больше и больше листов фольги вместе – тем вероятнее частицы, запущенные в неё, столкнуться с чем-либо, потеряют энергию, отскочат, изменят направление движения или даже остановятся. То же было бы верно, если бы вы наслаивали одну за другой проволочные сетки (рис. 6). И, как вы понимаете, из того, насколько далеко средняя галька может проникнуть сквозь слои сетки и насколько велики разрывы в сетке, учёные могут подсчитать на основании пройденной электронами или атомными ядрами дистанции, насколько атом пустой.
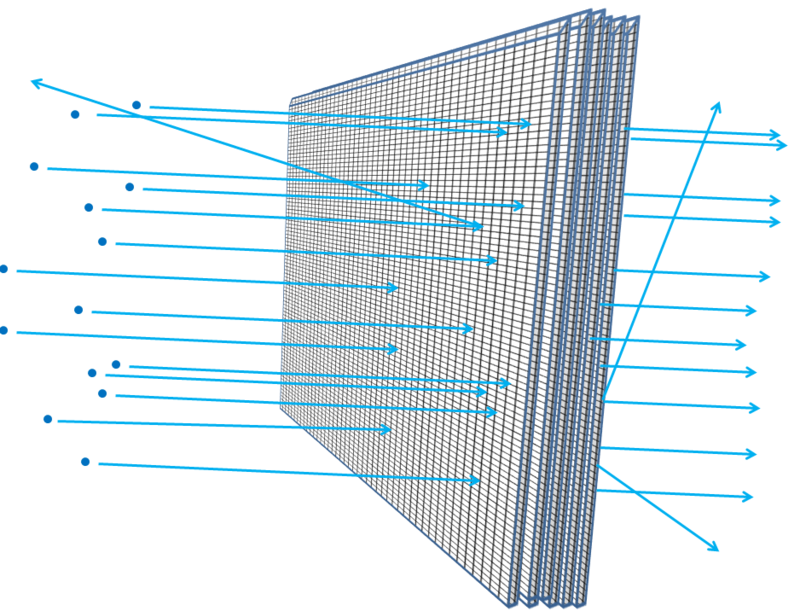
Рис. 6
Посредством таких экспериментов физики начала XX века установили, что внутри атома ничто – ни атомное ядро, ни электроны – не может быть большим, чем одна тысячная миллионных миллионных долей метра, то есть в 100 000 раз меньше самого атома. То, что такого размера достигает ядро, а электроны по меньшей мере в 1000 раз меньше, мы устанавливаем в других экспериментах – например, в рассеянии высокоэнергетических электронов друг с друга, или с позитронов.
Чтобы быть ещё более точным, следует упомянуть, что некоторые частицы потеряют часть энергии в процессе ионизации, в котором электрические силы, действующие между летящей частицей и электроном, могут вырвать электрон из атома. Это дальнодействующий эффект, и столкновением на самом деле не является. Итоговая потеря энергии значительна для летящих электронов, но не для летящего ядра.
Вы можете задуматься над тем, похоже ли то, как частицы проходят сквозь фольгу, на то, как пуля проходить сквозь бумагу – расталкивая части бумаги в стороны. Возможно, первые несколько частиц просто расталкивают атомы в стороны, оставляя большие отверстия, через которые проходят последующие? Мы знаем, что это не так, поскольку мы можем провести эксперимент, в котором частицы проходят внутрь и наружу контейнера, сделанного из металла или стекла, внутри которого вакуум. Если бы частица, проходя через стенки контейнера, создавала отверстия по размеру превышающие атомы, тогда внутрь устремились бы молекулы воздуха, и вакуум бы исчез. Но в таких экспериментах вакуум остаётся!
Также довольно легко определить, что ядро – это не особенно структурированная кучка, внутри которой нуклоны сохраняют свою структуру. Об этом уже можно догадаться по тому факту, что масса ядра очень близка к сумме масс содержащихся в нём протонов и нейтронов. Это выполняется и для атомов, и для молекул – их массы почти равны сумме масс их содержимого, кроме небольшой коррекции на связывающую энергию – и это отражено в том факте, что молекулы довольно легко разбить на атомы (к примеру, нагрев их так, чтобы они сильнее сталкивались друг с другом), и выбить электроны из атомов (опять-таки, при помощи нагрева). Сходным образом относительно легко разбить ядра на части, и этот процесс будет называться расщеплением, или собрать ядро из более мелких ядер и нуклонов, и этот процесс будет называться синтезом. К примеру, относительно медленно двигающиеся протоны или небольшие ядра, сталкивающиеся с более крупным ядром, могут разбить его на части; нет необходимости, чтобы сталкивающиеся частицы двигались со скоростью света.
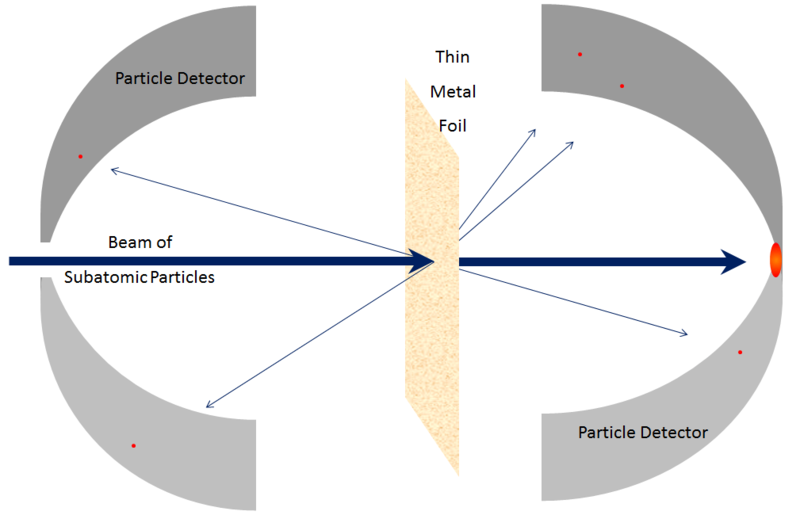
Рис. 7
Но чтобы понять, что это не является неизбежным, упомяну, что этими свойствами не обладают сами протоны и нейтроны. Масса протона не равняется примерной сумме масс содержащихся в нём объектов; протон нельзя разбить на части; а для того, чтобы протон продемонстрировал что-нибудь интересное, необходимы энергии, сравнимые с энергией массы самого протона. Молекулы, атомы и ядра относительно просты; протоны и нейтроны чрезвычайно сложны. опубликовано econet.ru
Если у вас возникли вопросы по этой теме, задайте их специалистам и читателям нашего проекта здесь.
P.S. И помните, всего лишь изменяя свое потребление - мы вместе изменяем мир! © econet
Источник: https://econet.ua/
Понравилась статья? Напишите свое мнение в комментариях.Подпишитесь на наш ФБ: , чтобы видеть ЛУЧШИЕ материалы у себя в ленте!

Добавить комментарий